IsótoposdeHidrógeno1 Pisapapeles

Es un metal de transición blando, brillante, amarillo, pesado, maleable y dúctil. El oro no reacciona con la mayoría de los productos químicos, pero es sensible y soluble al cianuro, al mercurio, al agua regia, al cloro y a la lejía. Este metal se encuentra normalmente en estado puro, en forma de pepitas y depósitos aluviales.
cuantos electrones tiene un atomo de oro?? Brainly.lat

Propiedades: La densidad del oro es 19,3 veces la del agua a 20ºC (68ºF), tal que 1 m 3 de oro pesa cerca de 19 000 kg (1 pie 3, unas 1200 libras). Las masas del oro, al igual que otros metales preciosos, se miden en la escala Troy, la cual contiene 12 onzas por libra. Se funde a 1063ºC (1947.97ºF) y ebulle a 2970ºC (5180ºF).
Oro (Au). Diagrama de la composición nuclear y configuración de electrones de un átomo de oro
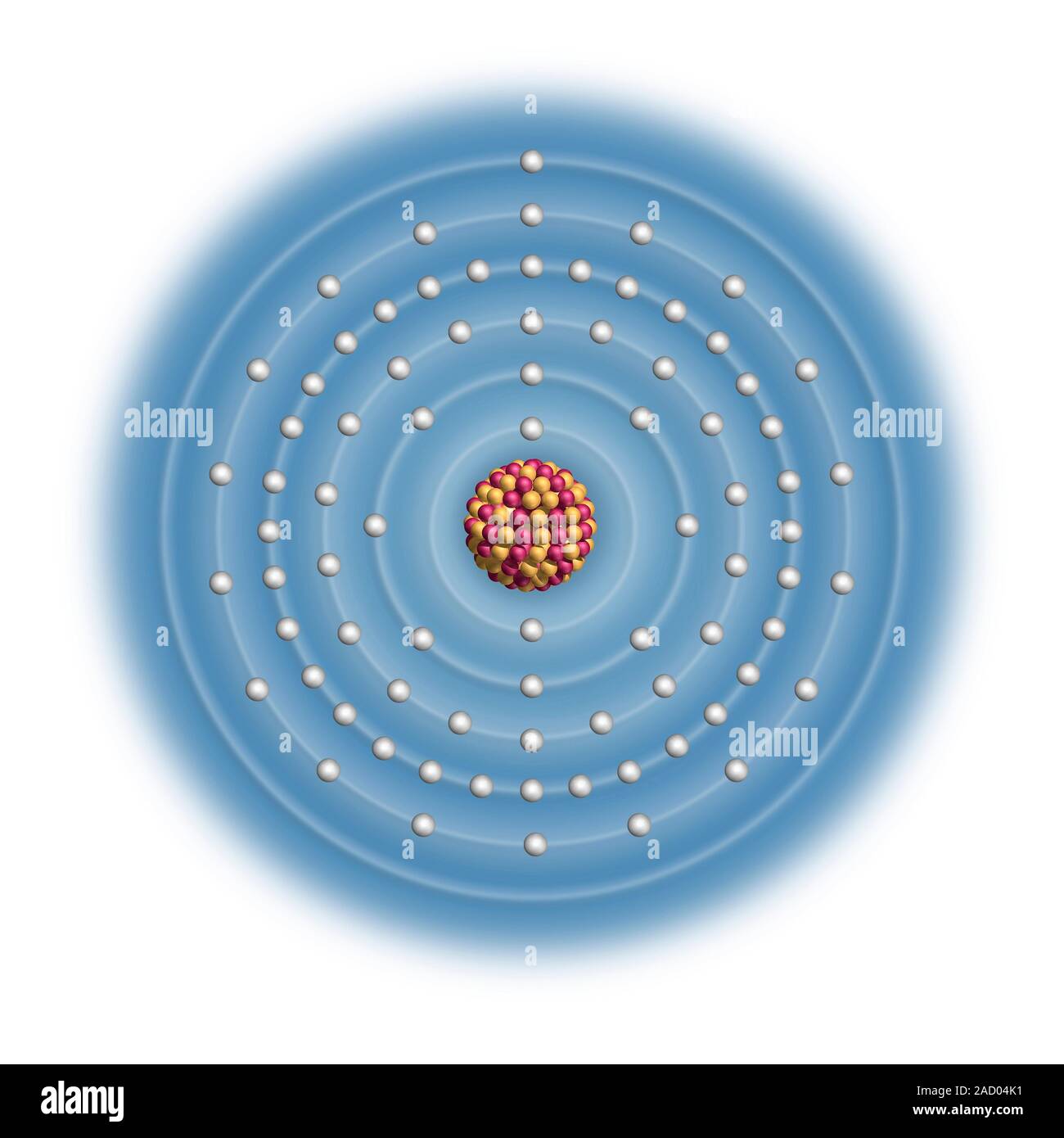
Oro. Radioactivo. No. El origen del símbolo Au viene de la palabra latina aurum que significa oro. Estructura cristalina. Cúbica centrada en las caras. Historia. Se conocen piezas arqueológicas de oro procedentes del neolítico tanto con fines ornamentales como utilitarios. Fue utilizado profusamente por los etruscos, los asirios y los.
Tabla Periodica Con Protones Neutrones Y Electrones The Best Porn Website

Átomos de oro estables que tienen el mismo número atómico que el elemento oro, pero difieren en el peso atómico. Au-197 es un isótopo estable.
Qué es un Isótopo Definición de Isótopo

Dureza (Mohs): 3,0. Punto de fusión: 1064 ºC. Punto de ebullición: 2856 ºC. Densidad: 19300 kg/m3. Isótopos: 197Au. Propiedades: El Oro es un metal precioso de color amarillo brillante. Es blando y no reacciona con la mayoría de elementos y compuestos. Aparte de la orfebrería, el oro es utilizado en la industria y la electrónica.
Oro Tabla periódica y Propiedades atómicas

Descriptor en español: Isótopos de Oro. Español de España. Descriptor. isótopos del oro. Nota de alcance: Átomos estables de oro que tienen el mismo número atómico que el elemento oro pero difieren en peso atómico. Au-197 es un isótopo estable del oro.
¿ Los isótopos son naturales y comunes? Brainly.lat

Anexo. : Isótopos de oro. El oro posee un peso atómico muy grande pero únicamente un isótopo estable, el 197 Au, y 37 radioisótopos, siendo el 195 Au el más estable de ellos con una vida media de 186 días. Actualmente el oro es considerado el elemento monoisotópico más pesado (antes se consideraba al bismuto como el elemento.
Oro (Au). Diagrama de la composición nuclear, la configuración de los electrones, los datos

Conocer el significado de isótopos y masas atómicas. El modelo nuclear del átomo de Rutherford ayudó a explicar por qué los átomos de diferentes elementos exhiben un comportamiento químico diferente. La identidad de un elemento se define por su número atómico (Z), el número de protones en el núcleo de un átomo del elemento.
Oro (Au). Diagrama de la composición nuclear y configuración de electrones de un átomo de oro
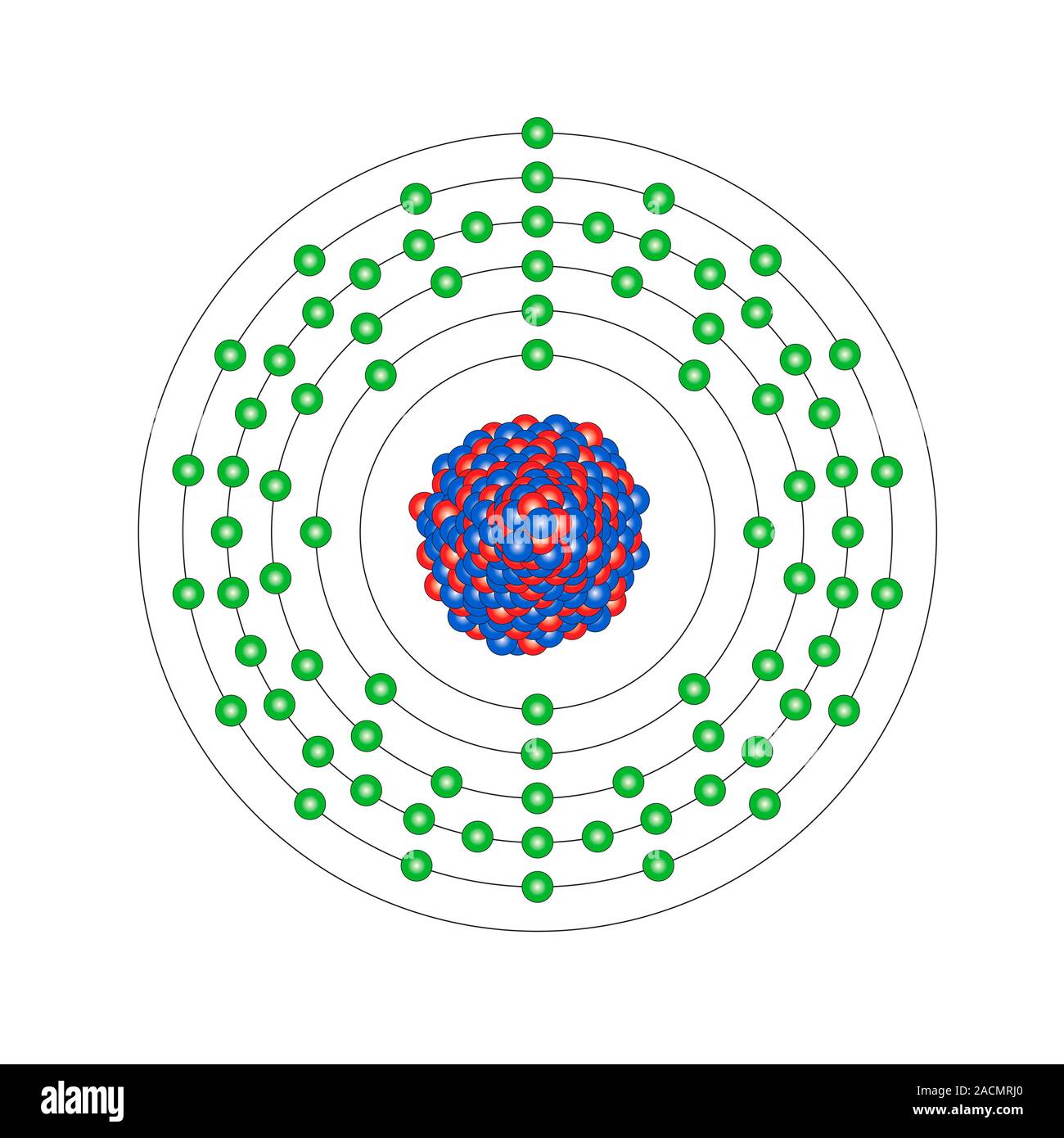
De Wikipedia, la enciclopedia encyclopedia. El oro posee un peso atómico muy grande pero únicamente un isótopo estable, el 197 Au, y 37 radioisótopos, siendo el 195 Au el más estable de ellos con una vida media de 186 días. Actualmente el oro es considerado el elemento monoisotópico más pesado (antes se consideraba al bismuto como el.
Isotopos
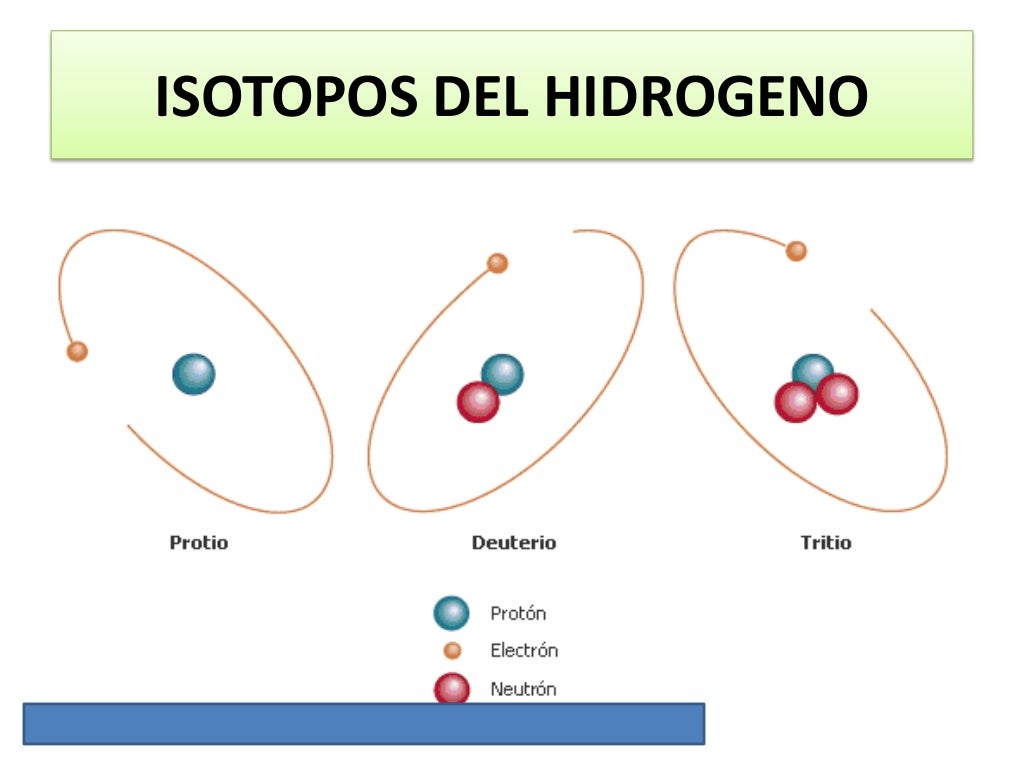
El oro es un elemento químico de número atómico 79 situado en el grupo 11 de la tabla periódica.Su símbolo es Au (del latín aurum).. Es un metal de transición blando, brillante, amarillo, pesado, maleable, dúctil (trivalente y univalente) que no reacciona con la mayoría de productos químicos, pero es sensible al cloro y al agua regia.El metal se encuentra normalmente en estado puro y.
¿Cuántos isótopos de oro hay? 2024

El oro es uno de los pocos elementos que se pueden encontrar en su estado nativo. El oro es el metal más maleable y dúctil. una onza de oro puede batirse a 300 pies 2 o estirarse en un cable de 2000 kilómetros de largo (1 μm de espesor).; El punto de fusión del oro es un valor asignado, que sirve como punto de calibración para la escala de temperatura internacional y la escala de.
El ORO Características y Extracción Minera
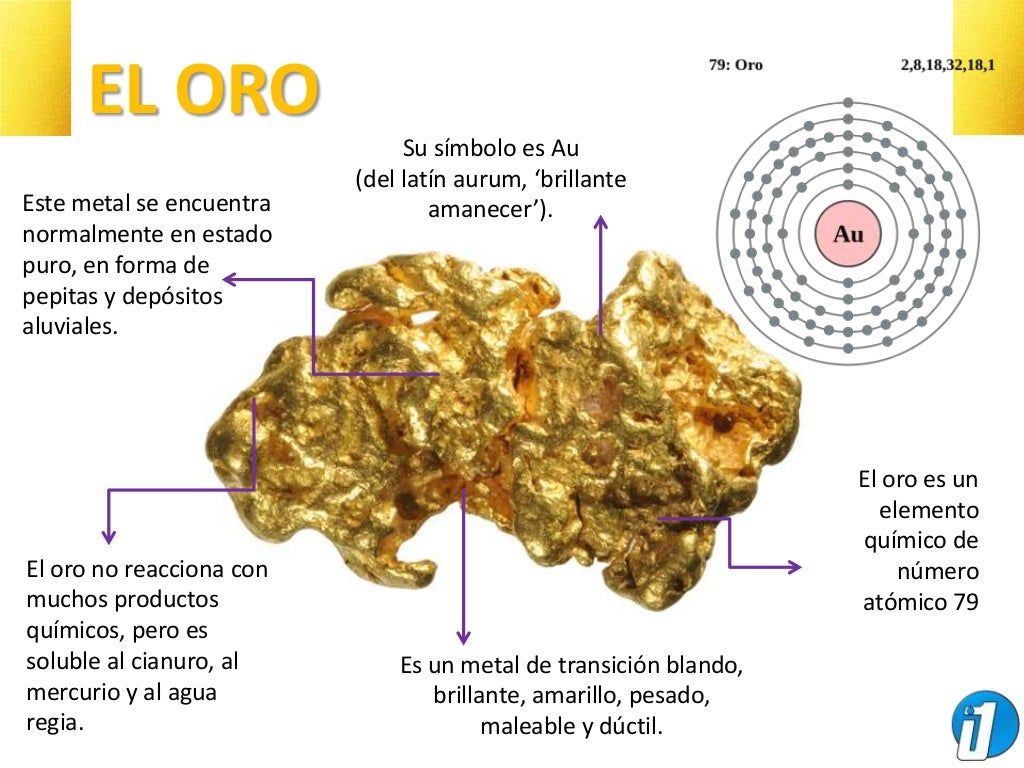
Anexo. : Tabla de los isótopos. Los periodos de semidesintegración de cada núcleido se indican según el color de cada celda. Los bordes coloreados indican los periodos de semidesintegración de los isómeros nucleares más estables.
Todos conocemos los colores más habituales del oro, comenzando por el clásico amarillo y

Sin embargo, la masa atómica de un átomo en general será muy cercana a su número de masa aunque tendrá algunas diferencias en los decimales. Debido a que los isótopos de un elemento tienen diferentes masas atómicas, los científicos también pueden determinar la masa atómica relativa (denominada algunas veces peso atómico) de un elemento.
Estructura de los átomos La tabla periódica (página 2)

El oro es un elemento químico de número atómico 79, que está ubicado en el grupo 11 de la tabla periódica. Es un metal precioso blando de color amarillo. Su símbolo es Au. Es un metal de transición blando, brillante, amarillo, pesado, maleable y dúctil. El oro no reacciona con la mayoría de los productos químicos, pero es sensible y.
Cuál es la fórmula química del oro y cómo se representa

El oro tiene un número atómico de 79 y un peso atómico de 196.967. El oro se representa con el símbolo 'Au' en la tabla periódica de los elementos. Se ubica entre los metales de transición, en el grupo 11 de la tabla, entre el platino y el mercurio.. El oro tiene número atómico 79, un peso atómico de 196.967 u y un peso específico de aproximadamente 19,3 gr/cm 3.
El Oro (Au) es un metal noble que posee 79 protones. Si uno de sus isótopos presenta 118

El oro es un elemento químico de número atómico 79, lo que significa que cada átomo de oro cuenta con 79 protones en su núcleo atómico. Se representa con el símbolo Au debido a la traducción de su nombre en latín aureum, es decir, "amanecer radiante". Se encuentra en el grupo 11 y el periodo 6 de la tabla periódica, por lo que.